[미생물 시험]
1. 배지 유효성 시험
1) 목적 : 제약 시험에 사용되는 미생물 배지의 적합성을 확인, 주문한 배지가 유효한지 확인하는 시험
2) 적용범위
- 무균 시험용 배지
- 미생물한도 시험용 배지
- 환경모니터링 시험용 배지
- 제조용수 시험용 배지
- 기타증균, 확인, 선택배지
3) 실시 주기
- 상용 조제배지: 입고 시 해당 Lot에 따라 시험 (Lot 마다 시험해야 하기 때문에 같은 Lot 배지로 주문)
- 조제배지: 구입시, 조제시 시험
4) 시험원칙
- 미생물 배지에 대한 새로운 제조번호마다 시험
- 시험대상 배지에 소량의 미생물을 접종
- 표준기관의 분양으로부터 5회 이하 계대 배양된 미생물을 사용
- 약전에 기재된 표준 미생물을 사용
2. 제조용수 시험
1) 제조용수의 종류
- 상수 (City water): 보통 수돗물
- 전처리수 (Pre-treatment water): carbon filter, reverse osmosis, eletrodeionization,
distillation 장치를 통과하기 전 및 통과 직후의 물
- 정제수 (Purified water): 상수를 역삼투, 이온교환에 의해 정제한 물
- 주사용수 (Water for injection): 정제수를 증류 또는 초여과하여 만든 물
- 청정증기 (Pure steam): 정제수를 증기제조장치를 사용해 제조한 증기
2) 시험항목 및 기준

엔도톡신, 미생물 시험항목 = 미생물 QC 업무
3) 미생물 시험법
(1) Pour plate (주입 평판법)
(2) Spread plate (평판 도말법)
(3) Membrane filtration (멤브레인 필터법) -> 보통 권장하는 방법
(4) MPN (Most probable number test) : 혼탁 정도나 빛 변화 등으로 미생물 증식의 수 판정
4) 정제수 미생물 시험 방법
① 멤브레인 필터가 장착된 여과기에 정제수 주입 후 여과
② 멤브레인 필터를 핀셋을 이용해 꺼내어 R2A Agar 표면에 놓음
③ 검액 여과하지 않은 필터를 R2A Agar에 놓아준 후 음성대조군으로 함
④ 30-35도 에서 5일간 배양
3. 무균 시험 : 가장 중요한 시험, 대한민국 약전 내용 참고
- 무균이 요구되는 원료/자재/제제 등의 미생물의 존재 유무를 확인하는 시험
- 각 국가 공정서의 조화(harmonized): USP <71>, EP<2.6.1>, JP<4.06>,KP<11>
- 무균시험 적합: 단지 이 시험조건에서 시험한 검체 중 오염미생물이 검출되지 않았음 (Batch 미포함)
1) 시험에 필요한 최소 검체수

2) 무균시험시 최소 검체 채취량
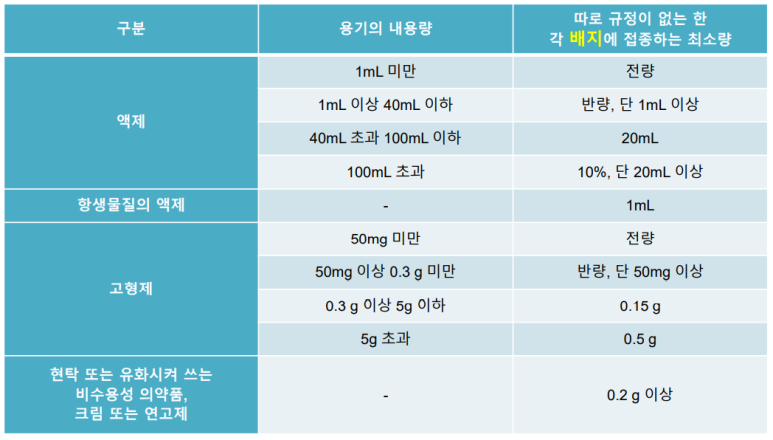
3) 무균시험 일반조건
(1) 시험 환경
: 무균조건 (ex. Isolator, "ISO 14644-1"의 Class 5(A grade))이며, 정기적으로 모니터링 필요
(2) 시험 준비
: 오염을 피하기 위한 예방조치는 검체의 미생물 검출에 영향을 주어서는 안됨
(3) 시험 시약 및 기구
: 배지는 무균성 및 성능이 확인되어야하며, 시약과 기구는 멸균되어야 함

(4) 시험 방법
: 검체의 특성에 따라 멤브레인 필터법과 직접법으로 구분
: 측정법의 적합성이 검증된 방법으로 수행해야 함
4) 무균시험 방법


멤브레인 필터법(TSB,FTM)과 직접법(TSB,FTM)
5) 시험결과 판정 방법
- 배양기간 중, 그리고 최종일(14일 이상)에 육안으로 미생물 증식 유무를 확인 (탁도 비교)
- 검체가 혼탁하여 판정이 어려울 경우, 기존 배지를 새 배지에 이식하여 4일이상 배양 후 판정
** 만약 균이 증식할 경우
-> 검체와 관계없는 원인이며, 시험이 무효함을 증명할 수 있을 경우에 한해 재시험 수행
-> 시험 무효화를 증명할 수 없을 경우에는 무균시험 부적합 판정
6) 무균시험 방법(멤브레인 필터법, 직접법) 비교 분석

7) 무균시험 장비
- Isolator, 과산화수소 훈증기(VHP)
- Equinox pump
[미생물 한도 시험]
* 미생물 한도 시험 = 생균수 시험 + 특정 미생물 시험
목적: 비무균의 원료 또는 제제가 규정된 미생물학적 품질 규격에 적합한지 여부를 판정하기 위함

1. 생균수 시험
1) 사용배지
- TAMC(Total Aerobic Microbial Count), TYMC(Total Yeast and Mold Count)

2) 시험법
- 멤브레인 필터법: 여과가 가능한 제제 (정확도 가장 높음)
- 한천평판혼합법: 모든 제제 가능 (시험량이 많을 경우 효율적), 액체상태의 고체배지, 멸균된 페트리디쉬
- 한천평판도말법: 모든 제제 가능 (시험량이 적을 경우 효율적), 고체 배지, 멸균된 스프레더
- 최확수법: 다른 방법의 이용이 불가능할 경우, 액체 배지(TSB)
2. 특정미생물 시험
: 규정된 조건에서 검출할 수 있는 특정 미생물(정상균총 or 유해 미생물)이 존재하지 않거나,
그 존재가 한정적인지를 판정하는 방법
1) 시험 항목 -(7)
- 담즙산 저항성 그람 음성균
- 대장균 (E. coli)
- 살모넬라 (Salmonella)
- 녹농균 (Pseudomonas aeruginosa)
- 황색포도상구균 (Staphylococcus aureus)
- 클로스트리디아 (Clostridia)
- 칸디다 알비칸스 (Candida albicans)
2) 검출 금지 항목
- 경구액제 (대장균)
- 외용제 (녹농균, 황색포도상구균)
- 좌제 (효모, 진균)
- 천연 동식물 유래 의약품 (살모넬라)
3) 용어의 정리
** 정상균총(Normal flora)
: 인체 내 존재하고 공생하는 미생물의 집단
: 피부 점막에 존재하며, 대체로 일정 상태로 숙주(인간)사이에 조화를 유지하며 병원균의 감염을 막음
** 선택 배지(Selective media)
: 두 종류 이상의 미생물이 혼합되어 있는 검체에서 원하는 미생물을 선택적으로 분리 배양하는데 사용
: 색소, 중금속, 항균제 등 원하지 않는 미생물의 증식을 억제하는 물질 함유
** 감별 배지(Differential media)
: 순수 배양된 미생물의 특정한 효소 반응을 확인하여 균종의 감별과 동정을 하기 위한 배지
: 감별이 용이하도록 지시약 등의 화학 물질 첨가
[엔도톡신 시험]
1. 엔도톡신의 정의
: 그람 음성균의 세포벽 구성 성분
: 극히 미량에서도 강한 발열 활성을 나타내는 내열성의 독소
* 엔도톡신 시험의 목적
- 엔도톡신은 어디에나 존재하는 물질로, 먹거나 마시는 것은 인간에게 해를 주지 않으나
혈액 내로 직접 들어가게 되면적은양으로도 발열및 부작용 일으킴
=> 때문에 혈관으로 직접 투여하는 주사제나 체내에 삽입하는 의료기기는 출하 승인 전에
존재 유무를 시험해야 함
2. 엔도톡신 시험법
: 참게의 혈구추출성분으로 만든 라이세이트(Lysate) 시약을 이용하여
그람음성균에서 유래되는 엔도톡신을 검출 또는 정량하는 방법

3. 엔도톡신 시험 장비 (Kinetic, Rapid kinetic)

4. 엔도톡신 시험 주의사항
1) 오염을 피하여 시험 진행
- 시험 도구 (Loading 전 96Well plate 이물 여부 확인) 오염 여부 확인 후 진행
2) PTS 카트리지에 Loading시 cell에 직선으로 Loading 하지 않도록 주의
- 일부 샘플이 먼저 주입되어 CV 값이 벗어날 수 있음
3) Splash out!! Bubble !! 주의
- 오염과 잘못된 흡광도가 측정 될 수 있음
4) 시험자 숙련도
[BI 시험]
1. BI 시험의 정의
- 모니터링 하고자 하는 멸균 절차에 강한 내성을 가지는 미생물종(박테리아 포자)으로 구성된 운반체 혹은
현탁액으로, 미생물이 접종된 운반체를 잘 유지하도록 디자인된 패키지나 운반 장치에 담겨 있음
- 해당 멸균방법에 내성이 가장 큰 표준화된 생존 미생물 균주를 이용한 멸균감시방법으로 멸균을
확인할 수 있는 가장 확실하고 신뢰할 수 있는 방법

- 세균아포를 포함한 모든 미생물의 생존여부를 확인
- 멸균 여부 증명
2. BI 시험에서 포자 사용
1) Geobacillus stearothermophilus 포자: 스팀멸균, 과산화수소멸균, Propylene oxide 멸균
2) Bacillus Atrophaeus 포자: 포르말린, Ethylene oxide 멸균
[DI (Data Integrity) ]
* DI 공통 기술 내용 - (PIC/S, WHO, MHRA)
- 데이터 기록 시점에 작성 일자를 함께 기록
- 문서 발행 내역은 추적될 수 있어야 함 (문서 번호 부여)
- 원본과 사본은 구분될 수 있어야 함
- 데이터는 실시간으로 생성되어야 함
- Data Integrity를 관리하기 위한 자사 정책 필요 (Data Governance)
- 데이터 변경이 필요할 경우 수정액이 아닌 실선으로 변경사유, 이름, 날짜를 기록
- 문서는 발행권한이 주어진 자에 의해서만 발행 되어야 함
- 기록된 데이터에 대한 2차 검토자가 필요
* ALCOA +
1) Attributable - 기인성 (출처)
: 데이터에 대한 추적성
2) Legible - 가독성
: 모든 데이터는 읽을 수 있어야 함
3) Contemporaneous - 동시성
: 행위와 동시에 데이터가 생성되고 기록되어야 함
4) Original - 원본성
: 원본 데이터는 보존되어야 함
5) Accurate - 정확성
: 데이터를 바꾸어서는 안됨
6) +
① Complete - 완전성
② Consistent - 일관성
③ Enduring - 지속성
④ Available - 활용성
'미생물' 카테고리의 다른 글
| [KTL교육] 미생물 품질관리 및 기초 미생물학 (2) (0) | 2022.12.27 |
|---|---|
| [KTL교육] 미생물 품질관리 및 기초 미생물학 (1) (0) | 2022.12.27 |

